�ȵ��ص��ٴ����Ӧ���ڿ�ѧ
2021-04-30 ��������
�ȵ������������ڵ��ȵ���ϸ������Դ�Ի���Դ�������������ǡ����ǡ����ǡ������ᡢ�ȸ�Ѫ���صȵĴ̼������ڵ�һ�ֵ����ʼ���,�ǻ�����Ψһ����Ѫ�ǵļ���,ͬʱ�ٽ���ԭ��֬���������ʺϳɡ�
�ȵ�����Ϊ������Ʒ,�ṹ����,������Զ������ͨ��ѧҩ;���������������������;������ҽ����еע�䷽ʽ��ҩ;�ǵ��͵ĸ������ɱ����߷��ղ�Ʒ�������й�ҩѧ��ҽԺҩѧרҵίԱ����ҩ��ȫר���鷢�����й��߾�ʾҩƷ�Ƽ�Ŀ¼2019�桷,Ƥ��ע���ȵ��ر�������35�־�ʾҩ�
�����ҹ���������������,�ȵ��ص��ٴ�Ӧ�úͿ�ѧ���������ע�����Ľ����ȵ��ص��ٴ�Ӧ����������ٴ������������Ӧ��������������������ȵ����Ƽ��ٴ�Ӧ�õ���״����ս��
�ȵ��ص��ٴ�Ӧ�������
1.1 ���ٴ���,�ȵ��������ǿ��Ƹ�Ѫ�ǵ���Ҫ�ֶΡ�
a. �ٴ�Ӧ�ó���
1���������ڷ���ʱ����Ҫ�ȵ�������,��������Ҫ�ȵ���������������Ƹ�Ѫ�ǡ�2���������䲻��Ҫ�ȵ�����ά������,�����ڷ�����ҩЧ�����ѡ���ҩ����ڿڷ�ҩʹ�ý���ʱ,��ʹ���ȵ��ؿ��Ƹ�Ѫ��,�Լ���������֢�ķ���Σ�ա���ijЩʱ��,�����Dz��̽ϳ�ʱ,�ȵ������ƿ���ʱ����Ҫ�ġ���������Ŀ���Ѫ�Ǵ�ʩ��
b. ��ҩ�������廯
��ͬ��������,1�͡�2�͡��������ҩ�������ڲ���;ͬʱ,��ͬ�ȵ��ز�Ʒ�ļ������ҩʱ�䶼�����ԵIJ��졣���,�ȵ�������廯��ҩ����,ȷ����ȷ��ҩ,����ٴ�Ч����
�� ���껼���ȵ���ϸ�����ܡ��������ܼ���,ͬʱ����֢/�ϲ�֢�����ʽϸ�,��Ҫ���Ӹ��廯�Ĺ����;�ϸ������ҩ��
�� 1�Ͷ�ͯ�����������ߺ�����ϲ�������,�辫ϸ���ڸ�ҩ����ƽ����Ч�Ͳ�����Ӧ,����Ӱ��Ѫ�ǿ���ˮƽ,���¶�ͯ���������ٻ�,��������������̥�����η���������������1,2��
c. ����������
������ͨ����Ҫ����ע������,���������ԶԼ�������ת��������Ҫ��
�ȵ������������Բ��ֱ��Ӱ��Ѫ�ǿ���Ч��,����Ӱ�컼�ߵ�Ԥ�����Ӷ���ҽ�Ʒ��á��γ�������Ѫ�ǹ������ѵĶ���ѭ����
1.2 �ȵ����Ƽ���Ʒ�ٴ�Ч���IJ����Ż��ƶ�����»���
�ȵ����Ƽ���Ʒ�ٴ�Ч���IJ����Ż����ƶ�����»�����ʱЧ���͵���Ҫ����֮һ��
������Դ�ͽṹ,�ȵ����Ƽ��ɷ�Ϊ����Դ���ȵ���(��һ��)���������ȵ���(�ڶ���)���ȵ���������(������)�������ٴ�����֤��,�������ȵ�����������ģ���������ȵ��ط��ںͼ��ٵ�Ѫ�Ƿ����ķ����Է�����������ȵ��ء�����,�ȵ��������ﻹ�����ߵ������������ı����Ժ������,��Ҳ�ͽ�һ������˻��߶����Ƶ������ԡ�
����Э��ҽԺ����ά�ٽ��ڱ�ʾ:����ڶ����������ȵ����Ƽ����,�������ȵ�������������Ч�Ͱ�ȫ�Է����һ���õ������������������ȵ����������ܹ����õ�ģ��������������ģʽ,����������������Ҫ,Ѫ�ǿ��ƴ�������,�����Ѫ�ǵȲ�����Ӧ���ո��͡�����,�ȵ��������ﻹ����ע��ʱ�������������ŵ㡣��
�ٴ�ʹ����,��ͬ����ʱЧ���͵��ȵ����Ƽ������ص�(����һ),�����ȵ��ص������Ƽ�,����ҩƷ�Ƽ��IJ���Ҳ���ܻᵼ��ҩƷ�����ڵ�����ѧ���Ժ�����ѧ���ԵȵIJ�ͬ,ҩ������ѧ/ҩЧ����ѧ(PK/PD)�����������ȵ������õĻ���,ҽ������ݻ��ߵľ������,���ò�ͬ����ʱЧ���͵��ȵ����ƶ�������Ʒ�����
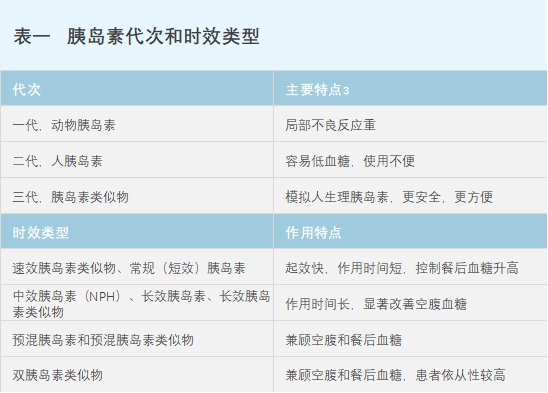
�ȵ��ص��ٴ����
���ϸ�����90���,�ҹ��ѿ�ʼ�����������ȵ����Ƽ���������,���Ų���ԭ���ȵ���������ר������,�ܶ೧�ҿ�ʼ��������ԭ���ȵ����������Ƽ�,��½�����С�Ŀǰ,�ҹ����еķ�ԭ���ȵ����Ƽ����ǰ���2007��ġ�ҩƷע������취���е�15�ࡰ���й���ҩƷ����������Ʒ�����е�,��δ������������ҩ��Ҫ���걨����,�Ƽ�����ٴ����������ע��
�������еġ������ָ�ȵ���������Ʒ����ͬͨ������ͬ����Ʒ�Ʋ�Ʒ֮������(Ʒ�����),��ͬͨ�����ȵ��ؼ������ϲ��ǡ������,Ϊ���ڲ���,������Ҳһ������(Ʒ�����)��
ͼ:Ʒ�ں�Ʒ�����,����Ի���������
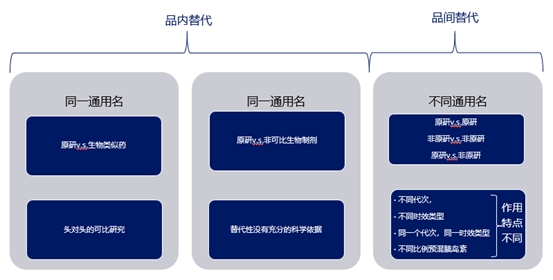
2.1 ͬһͨ����֮������(Ʒ�����)
a.ԭ�к���������ҩ�����:���Ʋ���ͬ
Ŀǰ,�й���û���ȵ�����������ҩ���С������ȵ�����������ҩ�Ŀ����������ȵ�����Ϊ������������Ʒ,�뻯ѧҩ���,������Է������ṹ���ӵ��ص�,���ٴ���Ч�ԡ���ȫ���ںܴ�̶��ϻ��ܵ��������������Ρ��������յȸ������ص�Ӱ�졣
�ִ������µ��ȵ���������������,ϸ�������ͷ��͡����롢�����ȶ�����������������ҩ��ҵһ�������ԭ��ҩ�ĺ��ļ������ؼ����Ƶ���������յ�������Ϣ,����������Ʒ������ϸ����������������ԭ�в�ͬ������ϸ������������,��ζ���ȵ�����������ҩ��ԭ���ȵ��ز�Ʒ������ȫ��ͬ��
ͬʱ,�ȵ��ض���Ҫ��ҩϵͳ(���ȵ���ע���,�õ�)�����ڻ��߿���ʹ�ò�ͬ�ĸ�ҩϵͳ,���һ����Ϊ,��������ҩ�ĸ�ҩϵͳ,PK/PD��α�ҩҲӦ�߶�����3��
b. ԭ�кͷǿɱ�������Ʒ�����:��������Ҫ��ѧ����
Ŀǰ�ҹ����еĹ����ȵ��ض��ǰ��ա����й���ҩƷ����������Ʒ(15��)������,��֤������ԭ�в�Ʒ�������ԡ�
���,������Ϊ,�������ķ�ԭ���ȵ��ز�Ʒ,ֻ����Ϊ����ԭ��Ʒ���к��걨��ͬ���Ʒ��,�ǿɱȵ�������Ʒ����
2.2 ��ͬͨ����������(Ʒ�����)
ҩƷͨ��������ͨ��һ��Ψһ�ġ�ȫ��ͨ�õġ�Ϊ��������������,Ҳ����ר������,��һ��ҩ�����ʻ���Գɷֵ�ʶ��4��Ҳ����,��ͬͨ���������˲�ͬ��ҩ�����ʺͻ��Գɷ֡�
��ͬͨ�������ȵ��������ص㲻ͬ��
�� ��ͬͨ�������ȵ�����������ڲ�ͬ����,��ô��ͬ�����ȵ��ذ�ȫ��Ч�Բ�ͬ,����һ���ȵ��ز�����Ӧ��,���������Ӱ�ȫ���㡣(���һ)
�� ��ͬͨ�������ȵ�����������ڲ�ͬʱЧ����,��PK/PD��ͬ,���Ч��Ч��Ч��,�ʺϿ��Ʋͺ�Ѫ��,���г�Ч�ȵ�������ʱ�䳤,���Բͺ�Ѫ�ǿ��Ʋ(���һ)
�� ��ͬͨ�������ȵ��ؼ�ʹ��ͬһ������,ͬһʱЧ���͵��ȵ���,����Чʱ��,���ʱ������õij���ʱ�䶼����ȫ��ͬ������,�Ŷ�,���������ȵ��ض����������ȵ����е���Ч�ȵ���������,�����ǵ�ѪҩŨ�ȴ��ʱ��ͳ���ʱ�䲻��ȫ��ͬ����ͬ����Ԥ���ȵ��ص�Ѫ���ȵ��ط�ֵˮƽ��ͬ,ҩ������ѧ����Ҳ������ͬ(��ͼ��)��
ͼ:�����ȵ��ؼ�������
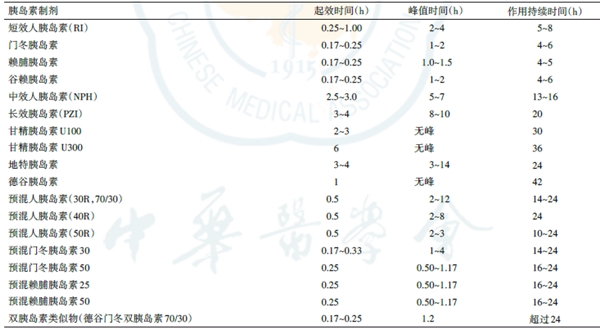
����Դ���й�2��������ָ�ϣ�2021��4�·����棩��
��Ȼ��ͬͨ�������ȵ�����Ӧ֢��ͬ,����ͬ����Ʒ�Ƶ��ȵ��ز�Ʒ������ߵ���������������ͬ,˵�����ж�����ߵİ�ȫ�Ժ���Ч�Ծ���˵��,���ͯ���и���,��������
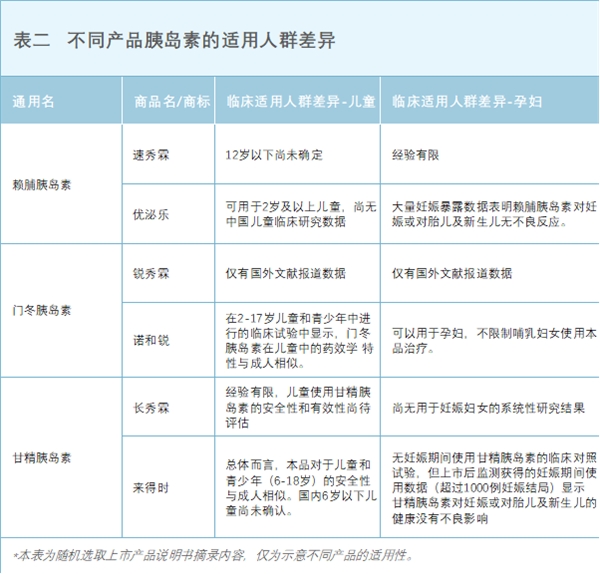
2.3 ���������ҽ�Ƽ��
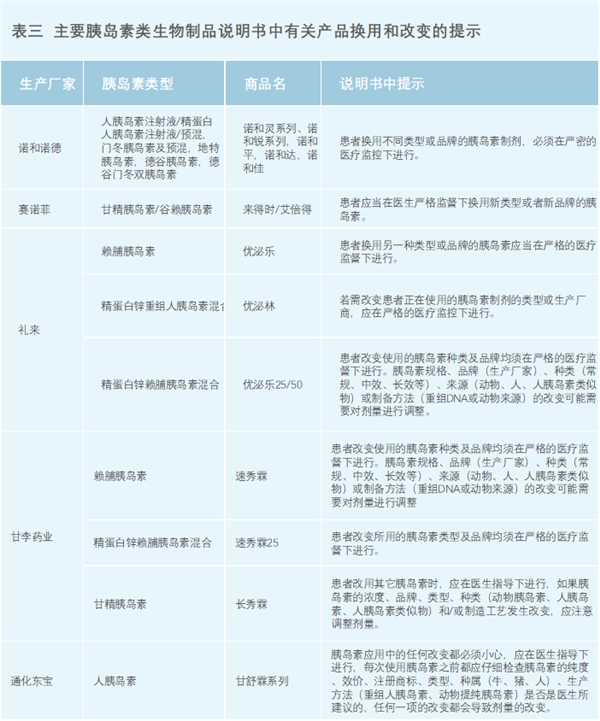
�����������۵��ȵ���˵�����϶��ἰ,��ͬƷ�ơ�����֮����ȵ���ת��ʹ��,��Ҫ�ϸ��ҽ�Ƽ��(������),Ӧ�ϸ��ջ�ҩ��ʾ����,���ϸ��ҽ�Ƽ��,��Ҫ�ļ���������,�����滻��
2.4 ҽ��ѡ��Ȩ�ͻ���֪��Ȩ
ҽ���ͻ��������Ʒ����ľ��߹�����Ӧ��������,ҽ�����Ʒ�����ѡ��������ȸ����ٴ���Ҫ�����ж�;����ҽ��Ӧ�뻼��Э��,�������������������ʾ,һ�����ϵ�ҽ����Ϊ��ҽ��ԭ���滻Ӱ�찲ȫ��Ч��5,����Ҳ���ڶ�浣��6,�ڴ�����¿���Ӱ�컼�����ơ�����Ҳ�е�����ʾ,Լ��1/4�������߲�Ը��������ȵ���,����Ҫԭ��Ϊ���Ľ���Ч��7��
���Ա�����Ϊ,�ٴ��滻��Ҫ���������ߵľ���������������������Ժ������Դ�����DZ����ҩ����;�����ٴ�������Ҫ,�����ٴ�ҽʦѡ��Ȩ�ͻ���֪��Ȩ;��ҩ��DZ�ڷ���Ӧ��˵������ǩ������ȷ��ʾ��������ٴ��滻�ڼ䷢�����ز����¼�,����Ӱ������Ч��,�������߲�����ҽ�ƾ��Ȳ�����
������Ӧ���������
��Բ�����Ӧ���ͷ�������,�й�������½����̨�����߷���,��ǿ��Ʒ��ȫ���,ȫ������ҩƷ����,����ҩƷ��ȫ����Ч�������ɿء�
�ȵ��������ٴ�Ӧ����,����ԭ��һֱ���ص�������һ������������ȵ��س������߲����ܶ������ȵ��ؿ���,������ܵ�����Ч���ͻ�ɥʧ,�����²���Ԥ֪�ĵ�Ѫ�Ƿ���,������־ֲ���ȫ���Գ�����Ӧ,����Σ�����߰�ȫ��
��ά�ٽ��ڱ�ʾ:���������з�ԭ���ȵ��������ṩ����ԭ�����ݶ������������������������ר����Ϊ �������ȵ��صIJ�����Ӧ���ع��ȵ���,�����������صIJ����¼������ʲ����ߡ�,����,���������ȵ��صĺ��������к�ȫ������ϵͳ��ҵ��ר�ҵĹ�ʶ��
�ܽ�
�ȵ��ص����ƴ�����խ,��Ҫ��ȷ�ļ�����ȷ����Ч�Ͱ�ȫ֮��ﵽ���ƽ�⡣
����Ŀǰ�ҹ��ȵ���������Ʒ,��δ�а�����������ҩ·�������еķ�ԭ�в�Ʒ,��˱�����Ϊ,���ٴ����Ӧ���ڿ�ѧ��ѭ֤��ԭ����к���ѡ��,��ϻ��߸��廯����,��ҽʦ��Ի��ߵľ�������������Ʒ�����������ת���з��ͣ�
������Դ:
���ǹ�. �й�1����������ָ��[M]. ��������������, 2012.
American Diabetes Association., Standards of Medical Care in Diabetes��2020. Diabetes Care, 2020. 43(Supplement 1): p. S1-S224
Docket No. FDA-2019-N-1132, Public Hearing - The Future of Insulin Biosimilars: Increasing Access and Facilitating the Efficient Development of Biosimilar and Interchangeable Insulin Products
�й�ҩ��2020,����,������Ʒͨ����������ԭ��
A. Teeple, L.A. Ellis, L. Huff, C. Reynolds, S. Ginsburg, L. Howard, D. Walls and J. R. Curtis,Physician attitudes about non-medical switching to biosimilars: results from an online physician survey in the United States,CURRENT MEDICAL RESEARCH AND OPINION,2019, VOL. 35, NO. 4, 611�C617.
A. Teeple, S. Ginsburg, L. Howard, L. Huff, C. Reynolds, D. Walls, L.A. Ellis and J. R. Curtis,Patient attitudes about non-medical switching to biosimilars: results from an online patient survey in the United States,CURRENT MEDICAL RESEARCH AND OPINION,2019, VOL. 35, NO. 4, 603�C609.
�ȵ��ػ����о�����,2020��10��������